美国食品药品监督管理局 FDA 监管约 7000 种不同的医疗器械产品,FDA 在医疗器械(Medical Devices)进口或拟进口至美国时,会验证并执行(Verifies and enforces)适用的医疗器械要求。FDA 根据医疗器械的分类及其风险程度,采用最少负担原则(Least burdensome approach)对医疗器械进行上市前审查(Premarket review),该审查基于对可靠的安全性与性能数据的全面评估,并采用全产品生命周期管理方法(Total product life cycle approach)。
CDRH 客户协作门户网站(CDRH Portal)
2022 年 10 月 3 日,FDA 宣布现在可以通过 CDRH 客户协作门户(Customer Collaboration Portal)网站"CDRH 门户"(CDRH Portal)在线提交 CDRH 电子副本 eCopy(Electronic copy)或电子提交模板与资源 eSTAR(Electronic Submission Template And Resource)上市前申报(Premarket submissions)文件。
FDA 创建并改进了CDRH 门户网站,以履行医疗器械用户收费修正案 MDUFA(Medical Device User Fee Amendments)IV 和 V 的规定。
基于 2021 年推出的 510(k) 申报进度跟踪器(Progress tracker for 510(k) submissions)和 2022 年 7 月推出的电子上传试运行流程(Trial process of electronic uploads),注册 CDRH 门户(CDRH Portal)帐户后,即可在线提交 CDRH eCopy 或 eSTAR 上市前申报(Premarket submissions)文件。
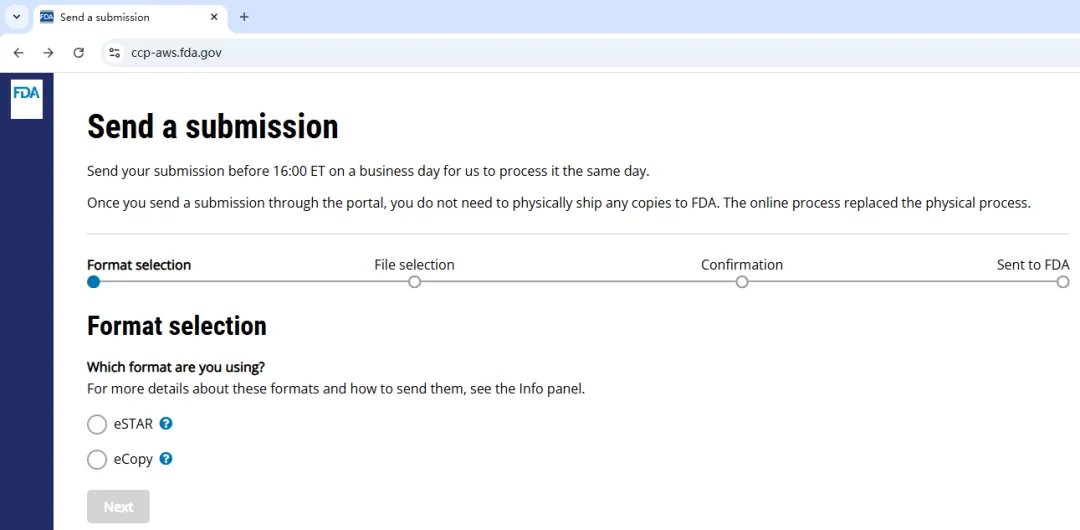
CDRH 使用 Okta 进行身份验证(Identity verification)和单点登录(Single sign-on),用户注册 CDRH 门户帐户时,系统会使用 Okta 服务。帐户注册和密码重置请求将来自以 @okta.com 结尾的电子邮件。
CDRH 门户(CDRH Portal)为 CDRH 上市前申报(Premarket submissions)提供进度追踪(Progress tracking)和在线提交(Online submission)功能。在线进度追踪器(Online progress tracker)有一个仪表板(Dashboard),显示近乎实时的提交状态。
所有由 CDRH 主导的上市前申报类型(Premarket submission types)均可在审查流程的任何阶段上传至 CDRH 门户网站。官方联系人(Official correspondents)在将电子申报(Electronic submission)上传至 CDRH Portal 门户网站后,无需再向 FDA 发送纸质附函(Physical cover letter)。
- 自 2023 年 10 月 1 日起,所有 510(k) 申报(510(k) submissions)(除非获得豁免)都必须通过 CDRH 门户网站使用 eSTAR 以电子方式提交。
- 自 2024 年 11 月 1 日起,所.........
美国食品药品监督管理局 FDA 监管约 7000 种不同的医疗器械产品
原文转载:https://www.kjdsnews.com/a/2553485.html
收藏篇!2024年美客多市场大促活动日历 收藏篇!2024年美客多市场大促活动日历 还在说展会获客难?!这份攻略一定要收藏! 2024年5月1日英国公司注册官费上调,抓住最后的注册时机! 如何注册一家香港公司?具有哪些优势? 卖家所有站点账号被"一锅端"! 【美国进口清关】CDRH 门户网站:在线提交医疗器械 eSTAR 和 eCopy 上市前申报 【美国进口清关】CDRH 门户网站:在线提交医疗器械 eSTAR 和 eCopy 上市前申报
没有评论:
发表评论